|
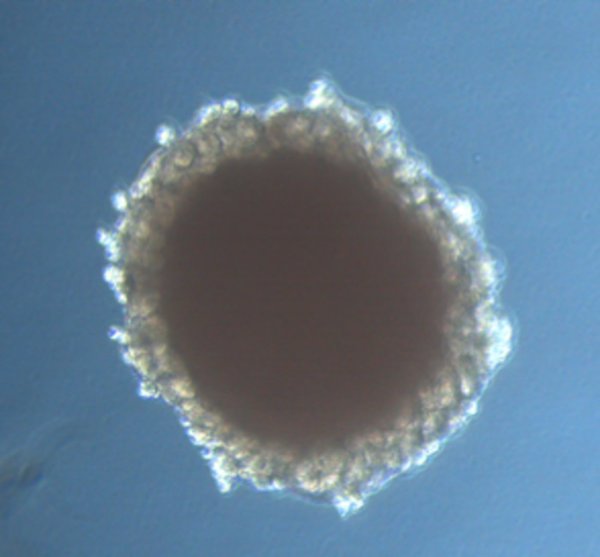
Un grupo de investigadores internacionales, entre los que se encuentran centros de investigación españoles, ha demostrado que los miniriñones diabéticos tienen una mayor susceptibilidad a la infección por SARS-CoV-2, así como evidencia genética del papel esencial del receptor ACE2 en COVID-19.
Además, han identificado que la programación metabólica provocada por la diabetes es crítica y aumenta la susceptibilidad a la infección por SARS-CoV-2 en el riñón. Estos resultados pueden conducir a la identificación de nuevas intervenciones en la patogenia de la COVID-19 dirigidas al metabolismo energético.
Esta una colaboración internacional, investigadores liderados por Nuria Montserrat, profesora de investigación ICREA en el Instituto de Bioingeniería de Cataluña (IBEC) e investigadora principal del grupo "Pluripotencia para la regeneración de órganos", han generado miniriñones humanos que simulan el riñón de una persona con diabetes en estadios iniciales de la enfermedad. Estos miniriñones diabéticos abren la puerta a estudiar, entre otros, la relación entre la diabetes y la COVID-19.
Desde hace dos años, miles de científicos y médicos de todo el mundo trabajan para entender cómo se desarrolla el COVID-19 y qué relación tiene con otro tipo de enfermedades. Diversos estudios indican que las personas con diabetes tienen más probabilidades de desarrollar COVID-19 grave, así como que más del 20% de los pacientes hospitalizados por COVID-19 sufren daño renal agudo. Sin embargo, hasta la fecha se desconocía cuál fue el factor que provocó que esto sucediera.
Ahora, el equipo internacional liderado por Nuria Montserrat en colaboración, entre otros, con investigadores de la Universidad de Florida, el Instituto de Ciencias de la Vida de la Universidad de Columbia Británica en Canadá, el Instituto Karolinska y el Hospital Universitario Karolinska en Suecia han utilizado la bioingeniería para desarrollar mini-riñones que simulan el riñón de una persona en las primeras etapas de la diabetes.
En esta colaboración internacional los investigadores han proporcionado, por primera vez, el uso de organoides renales para comprender las primeras etapas de la diabetes en este órgano. Para demostrar que el receptor ACE2 desempeña un papel esencial en la infección por SARS-CoV-2 en el riñón, el equipo también ha utilizado la ingeniería genética para generar organoides defectuosos para otros receptores descritos hasta la fecha como puertas de entrada del virus.
Utilizando células renales de pacientes, este estudio, publicado en revista 'Cell Metabolism', también revela el papel del metabolismo energético en la infección por SARS-CoV-2, abriendo la puerta a la identificación de nuevas intervenciones terapéuticas para tratar la COVID-19.
DESARROLLO DE LOS MINI-RIÑONES
Se han desarrollado mini-riñones en el laboratorio a partir de células madre humanas pluripotentes. Para reproducir el entorno diabético, los investigadores han sometido los miniriñones a condiciones de cultivo que dan como resultado la generación de miniriñones con las mismas características celulares y alteraciones metabólicas que los que se encuentran en los riñones de una persona con diabetes en etapa inicial.
Utilizando diferentes técnicas de biología molecular, como la edición de genes, los investigadores han observado que, en los miniriñones diabéticos, es la abundancia del receptor ACE2 la que determina la susceptibilidad a la infección viral, estableciendo una relación causal entre la diabetes y la presencia de uno de los receptores descritos hasta ahora como determinantes en la infección por SARS-CoV-2.
"Nuestro modelo de organoide renal diabético nos ha permitido observar que los miniriñones diabéticos, con un mayor número de receptores ACE2, tienen una mayor susceptibilidad a la infección viral", señala Elena Garreta, Instituto de Bioingeniería de Cataluña y primera coautora del estudio.
Para comprobar si los resultados obtenidos con los miniriñones también se observan en el órgano nativo, los investigadores analizaron células renales de pacientes con diabetes y de individuos sin diabetes. Los datos muestran que las células renales de pacientes diabéticos, al igual que sucede en los miniriñones, tienen más receptores ACE2 y sufren una mayor tasa de infección por SARS-CoV-2. Para profundizar en los mecanismos que pueden explicar tales observaciones, los investigadores utilizaron un compuesto que modula el estado metabólico de las células y encontraron que el tratamiento redujo la infección viral.
"Este hallazgo arroja luz sobre un mecanismo potencial detrás de los casos más graves de pacientes diabéticos. Esta tecnología mejorará nuestra capacidad para investigar cómo el virus interactúa con diferentes órganos del cuerpo humano", ha explicado Ali Mirazimi, profesor adjunto en Karolinska Institutet y uno de los autores correspondientes del estudio.
|




